Автор: Др. Артур Олсон, профессор, Исследовательский институт Скриппса
краткое изложение
В этом обширном обновлении лидер команды FightAIDS@Home, профессор Артур Олсон вкратце перечисляет без малого десятилетие прогресса в борьбе против СПИДа: новые вычислительные методы, новое понимание ключевых белков ВИЧ и огромные объемы вычислительных результатов, которые только начали изучаться. Несмотря на сворачивание Фазы 1, Фаза 2 этого громадного проекта будет продолжать продвигать жизненно важное исследование в самый смертельный вирус в мире.
Проект FightAIDS@Home (FAAH) присоединился к World Community Grid почти 10 лет назад и является самым его длинным непрерывно работающим проектом. Фаза 1 в настоящее время свертывается, так что это хороший момент, чтобы дать World Community Grid добровольцам резюме кто мы, какими были наши цели, какие вычислительные приближения были включены в вами предоставленные ресурсы и то, чего мы достигли к этому моменту. Мы постоянно осознаем, что это исследование возможно только из-за вашей невероятной щедрости, и мы надеемся, что вы все останетесь участниками Фазы 2 нашей работы.
Кто стоит за FightAIDS @ Home?FAAH, которая использует вычислительные исследования, чтобы помочь продвинуть поиск новых методов лечения против ВИЧ/СПИДа, начался с Entropia (ныне прекратившей свое существование платформы распределенных вычислений) в 2000 году, как сотрудничество между Скоттом Куровски, Тим Cusac, доктор Гаррет Моррис и мной. 21 ноября 2005 года FAAH присоединился к World Community Grid. В течение последнего десятилетия постоянно растущая вычислительная мощность, обеспечиваемая добровольцами World Community Grid, позволила нам расширить масштабы нашего исследования ВИЧ на много порядков значительности. В качестве дополнительного бонуса, эти огромные ресурсы также вдохновили нас на создание новых инструментов и стратегий, чтобы использовать потенциал, предоставляемый World Community Grid. Эти инструменты не только повышают эффективность и точность наших вычислений, управляемых исследований против ВИЧ, но также помогают развивать исследования, которые остальная часть научного сообщества продолжает в отношении других заболеваний.
Проект FightAIDS@Home работал в лаборатории Олсон по выделенной преемственности Postdoctoral Research Associates в течение последних 10 лет. Гаррет Моррис, Уильям "Линди" Линдстром, Алекс Перриман и Даниэль Сантьяго, по очереди брали на себя лидерство в проведении наших вычислительных экспериментов на World Community Grid. Им ассистировали на протяжении многих лет несколько членов лаборатории, включая Майкла Пике, Рут Huey, Стефано Форли, Саргиса Даллакяна Алекса Жилле и Макса Чанга. Как и в большинстве академических лабораторий, постдоки остаются на срок от 2 до 4 лет, а затем переходят на более долговременные позиции. Даниэль Сантьяго только что покинул лабораторию и мы в настоящее время интервьюируем на нового постдока, научного сотрудника, чтобы тот занял его место.
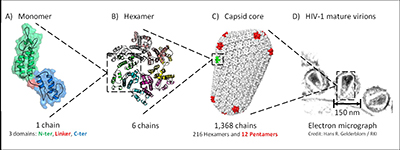
FightAIDS@Home целиВирус иммунодефицита человека (ВИЧ), вирус, который вызывает синдром приобретенного иммунодефицита (СПИД), заразил более 70 миллионов человек во всем мире с начала этой пандемии. В настоящее время более 35-ти миллионов человек инфицированы ВИЧ и более 2-х миллионов заражаются каждый год. Почти один миллион человек умирает от СПИДа каждый год, что делает ВИЧ самым смертоносным вирусом, который причиняет страдания человечеству.
Лаборатория Олсон заинтересована в понимании молекулярных механизмов, ответственных за развитие лекарственной устойчивости ВИЧ и в использовании этого понимания, чтобы помочь разработать новые терапевтические подходы для лечения ВИЧ-инфицированных лиц. Я руковожу центром, финансируемым NIH (National Institutes of Health), под названием HIVE (HIV Interaction and Viral Evolution) Center, который состоит из 14-ти отдельных лабораторий в 8-ми различных учреждениях по всей стране. Лаборатория Олсона, и кроме того проф. Рон Леви в Университете Темпл, участвуют в вычислительных аспектах задач Центра. Наш подход к проблеме лекарственной устойчивости в том, чтобы имитировать взаимодействие синтетических органических молекул с вирусными белками, для предсказания того, какие из них могли бы связывать и влиять на активность этих белков. Чтобы сделать это моя лаборатория разработала и использует две вычислительных программы AutoDock и AutoDock Vina для скрининга больших библиотек химических соединений. Основная цель этих вычислений - обнаружить какие соединения могут потенциально взаимодействовать и подавлять деятельность так называемого "дикого типа" и резистентных к лекарственным средствам мутации белков, которые развивались у пациентов. Основными белковыми мишенями для этой работы были ВИЧ-протеаза (PR), интеграза (IN) и обратная транскриптаза (RT). Это те три белка, для которых FDA имеет утвержденные препараты для лечения ВИЧ-инфицированных пациентов. Они также являются теми тремя ферментами, производимых вирусом, чтобы довести до конца химические реакции, которые поддерживают жизненный цикл вируса. Используя обширные структурные данные на диком типе и мутантных белках, а также мутационных данных лечащихся ВИЧ-инфицированных пациентов, мы исследуем гипотезы и отношения между молекулярной структурой и развитием лекарственной устойчивости. Вычислительные ресурсы World Community Grid внесли неоценимый вклад в расширение наших вычислительных подходов в этой научно-исследовательской работе.
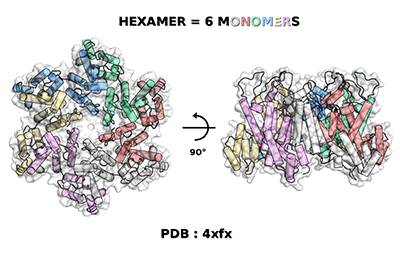
В первые годы FAAH, опыты, как правило, были вычислительно оценивающими несколько тысяч соединений против одного кармана одного типа вирусной структуры - с активным участком ВИЧ-протеазы. "Активный участок" является регионом, где химическая работа будет выполнена с помощью фермента. Протеаза ВИЧ рубит длинную, вирусную, мульти-белковую полипептидную цепь в нескольких различных, конкретных местах. Сокращение этой мульти-белковой цепь в различные кусочки, в дальнейшем позволяет этим различным индивидуальным белкам свернуться в их нормальные, зрелые формы, необходимые для их функционирования. Эти свернутые вирусные белки работают вместе, чтобы создать новые частицы ВИЧ, которые сбегут из инфицированной клетки, созреют, а затем заразят новые клетки, которые распространяют инфекцию внутри пациента и позволят инфекции распространиться к новым людям. Когда активность протеазы ВИЧ существенно нарушается, то эти мульти-белковые вирусные полипептидные цепи больше не разделены эффективным, хорошо упорядоченным образом. Это заставляет инфицированную клетку производить незрелые, нефункциональные частицы, неспособные инфицировать другие клетки. Очень важно, что когда ВИЧ препараты протеазы были объединены с ВИЧ препаратами обратной транскриптазы, смертность связанная с ВИЧ-инфекциями резко сократилась. До существования препаратов ВИЧ-протеазы, заражение ВИЧ было в основном быстрым и ужасным смертным приговором. Когда препараты ВИЧ-протеазы были объединены с другими классами анти-ВИЧ препаратов, чтобы сделать коктейли ВААРТ (Высокоактивная-антиретровирусная терапия), то многие ВИЧ-инфицированные пациенты смогли вести долгую и продуктивную жизнь с приемлемым качеством жизни. Тем не менее, поскольку ВИЧ продолжает развиваться в несколько разных форм, которые способны противостоять воздействию этих препаратов (то есть, новые мульти-лекарственно-устойчивые мутанты супербактерии продолжают появляться и распространяться), мы должны открыть для себя новые виды лекарственных препаратов и терапевтических вмешательств, которые смогут сделать эти мутанты непригодными.
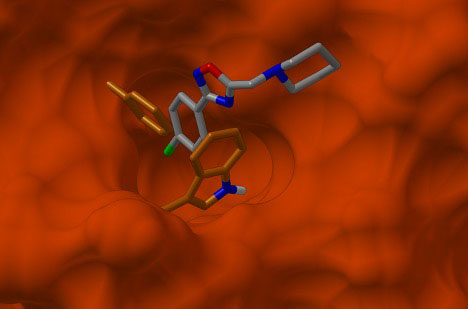
World Community Grid позволяет беспрецедентные вычислительные подходы для FAAHВычислительная проблема стыковки это высокоразмерный поиск возможных взаимодействий между двумя молекулами, химического соединения и вирусного белка-мишени. Надо, как правило, генерировать миллионы поз двух взаимодействующих молекул и для каждой позы вычислить энергию взаимодействия между ними. Эта оценка энергии осуществляется путем суммирования энергий взаимодействия между всеми атомами в двух молекулах. Когда мы впервые разработали AutoDock в 1990 году, одна стыковка занимала 20 минут или больше на самых быстрых компьютерах того времени. Сегодня, благодаря закону Мура, такой расчет может занять от несколько секунд до минуты в зависимости от сложности участвующих молекул. Таким образом, возможность скринить много молекул против конкретного белка-мишени (т.е. виртуальный скрининг) стала вероятной. Однако найти хорошего кандидата молекулу (хит), которая хорошо связывается с функциональным участком на белке требует скрининга очень большого количества химических соединений. Чем больше библиотека соединений, тем лучше шансы, что хорошое хит соединение будет в этой библиотеке.
Имея наш FAAH проект World Community Grid позволило нам запустить вычисления, которые заняли бы буквально сотни лет на более традиционных компьютерных системах. Теперь мы можем запускать виртуальные экраны химических библиотек против не одиночного белка-цели, но против больших выборок лекарственно-устойчивых мутантных белков этого вируса-цели. Вычислительная мощность World Community Grid также позволила нам увеличить размер библиотеки, которые мы используем в наших виртуальных скринах. Ранее мы были только в состоянии скринить библиотеки из нескольких тысяч соединений. Сегодня мы, как правило, скриним комбинированные библиотеки, содержащих более 5 миллионов соединений против каждого белка-мишени ВИЧ. Это дает нам гораздо больше шансов найти хорошие хитовые молекулы.
Одним из важнейших аспектов вычислительной стыковки - как взаимодействующие молекулы представлены или смоделированы. AutoDock был первым кодом стыковки, который позволил модели химического соединения быть гибкой при стыковке с белком-мишенью. Каждая связь в соединении, способная вращаться или поворачиваться, добавляла еще одно измерение в пространство поиска, которое должно было быть изучено, и поэтому, к сложности вычислений. В те дни целевой белок должен был рассматриваться как жесткая молекула, так как сложность его гибкости было бы слишком тяжело вычислительно смоделировать. Используя силу World Community Grid, мы смогли преодолеть это ограничение и внедрили различные представления гибкости белка, давая нам более реалистичные модели белка-мишени. До этого момента волонтеры FAAH пожертвовали более 340000 лет машинного времени для наших научно-исследовательских работ.
Научные достиженияПутем скрининга библиотек соединений против и дикого типа, и многочисленных лекарственно-устойчивых мутировавших версий ВИЧ-протеазы, мы смогли охарактеризовать спектр мутантов, которые существуют и объединить их в характерные варианты. Это дало нам возможность сократить количество прототипичных мутантов ВИЧ PR, которые мы должны использовать в наших виртуальных скринах и позволило нам и другим сосредоточить наше внимание на видах вариаций, которые вирус способен сделать, чтобы остаться функциональным в присутствии лекарственной терапии.
По мере увеличения числа добровольцев World Community Grid и суммы пожертвованной ими компьютерной мощности на протяжении многих лет, мы смогли значительно увеличить размер и сложность типов экспериментов, которые мы могли бы выполнять. Теперь мы пристыковали миллионы низкомолекулярных соединений против нескольких различных регионов всех ферментов, которые производит ВИЧ - протеазы, обратной транскриптазы и интегразы. Обратная транскриптаза ВИЧ является частью вирусного механизма, делающего новые копии его генетического материала. Он принимает РНК ВИЧ от первоначальной вирусной частицы и делает более стабильной ее версию ДНК (так называемая кДНК, или комплементарная ДНК). Интеграза ВИЧ затем обрабатывает вирусную ДНК, закрепив часть каждого ее конца, чтобы сформировать более реагирующие "липкие концы". Интеграза затем окончательно прикрепляет липкие концы ДНК вируса к человеческой ДНК, чтобы создать постоянно инфицированные клетки, которые затем идут на производство новых копий вируса. Таким образом, World Community Grid позволил нам вычислительно оценить миллионы соединений в отношении многих различных регионов всего вирусного механизма - вместо только возможности оценить тысячи соединений против одного региона одного типа фермента. Это займет у нас много лет, чтобы проанализировать эти горы данных, выбрать наиболее перспективные соединения-кандидаты и экспериментально оценить эти кандидаты в «мокрых» лабораторных экспериментах, выполненных нашими сотрудниками. Но мы создали новые инструменты, чтобы помочь нам обрабатывать и более эффективно анализировать эти данные, и мы разрабатываем дополнительные подходы, чтобы помочь нам собрать более полезную и более точную информацию из результатов, что добровольцы как вы сделали.
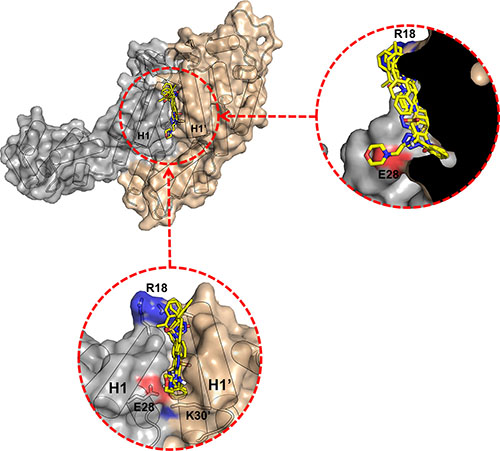
Совсем недавно, мы обратили внимание на концепцию синергетического ингибирования фермента ВИЧ функции. В дополнение к нацеливанию на активные участки этих ферментов, мы также смогли искать новые ингибиторы, которые связываются с "аллостерическими" участками на каждой из этих вирусных наномашин. Аллостерические ингибиторы были обнаружены и в интегразе ВИЧ и в обратной транскриптазе. Большинство ингибиторов отключает функцию фермента путем связывания непосредственно с "активным" (участок конкретного региона фермента, где происходит химическая работа) и блокирует его способность функционировать. 9 FDA-одобренных ВИЧ препаратов протеазы являются примером этих традиционных типов ингибиторов: они связываются с и блокируют активный участок в полом тоннеле в центре протеазы, который предотвращает возможность вирусного мульти-белкового полипептида связываться в пределах этого туннеля и расщепиться. Аллостерические ингибиторы работают в очень непохожей манере - они связываются с совершенно другим участком, регулируют конформационные предпочтения и/или гибкость всего целевого белка и тем самым отключают активный участок. Они связывают далеко от активного сайта и проецируют их влияние на остальную часть фермента. Аллостерические торможение, это как положить защелку на ручки ножниц для того, чтобы предотвратить лезвия от возможности открыться и закрыться и порезать что-то. Самое главное, различные эксперименты с ВИЧ, раком и малярией показали, что комбинации аллостерических ингибиторов и активных участков ингибиторов могут (а) сгенерировать комбинированную терапию, которая более эффективна против текущих супербактерий и что (б) на самом деле замедлит эволюцию новых лекарственно-устойчивых мутантов.
Нет известных аллостерических ингибиторов ВИЧ PR. Однако мы предположили, что могут существовать участки для аллостерического ингибирования HIV PR. Мы запускали FAAH виртуальные экраны против возможных участков и обнаружили, что есть химические соединения, которые могут связываться с этими участками. Эти наблюдения подкрепляются экспериментальными рентгеновских дифракционными экспериментами на PR в присутствии химического фрагмента библиотеки. Наблюдаемые в этих экспериментах 3 участка отдалены от активного участка ВИЧ PR, где химические фрагменты связываны. Мы теперь сосредоточились на поиске лучших связывающих соединений в этих участках, использующих наши виртуальные экраны FAAH. Некоторые из хитов из этих скринов были проверены рентгеновской кристаллографией и ЯМР-спектроскопией. Дальнейшее развитие и оптимизация этих хитов продолжается. Мы также тесно сотрудничаем с другими исследователями HIVE Центра, профессором Kvaskhelia в Университете штата Огайо и профессором Арнольдом в Университете Рутгерса по улучшению аллостерического ингибирования интегразы ВИЧ и обратной транскриптазы, соответственно.
Рафинированные результатыДругой подход к этой проблеме, которая была разработана в сотрудничестве с Лабораторией Леви в Университете Темпл, включает отдельный вычислительный шаг, оценивающий не только в топ соединений из виртуального скрина, но многие из топ ранговых соединений. Это вычисление использует сложные молекулярные приближения, основанные на динамике оценки свободной энергии связывания, которые слишком трудно вычислительно выполнить при стыковке, но которое может различать истинные и ложные последующие срабатывания к стыковке. Этот подход, называемый BEDAM, осуществляется с молекулярным инструментом моделирования под названием Academic IMPACT, который работает в фазе 2 нашего FAAH проекта на World Community Grid.
В целом, волонтеры World Community Grid сделали возможным бесценный ресурс для нашей постоянной работы в понимании природы лекарственной устойчивости ВИЧ. Как и в большинстве научных проектов, наряду с новыми результатами, возникают новые вопросы. Хотя у нас есть достаточно, чтобы получить полную картину эволюции лекарственной устойчивости ВИЧ или создать новый препарат, который побеждает сопротивление ВИЧ, мы разработали новые вычислительные методологии и открыли ряд направлений исследований, которые могут привести к лучшим приближениям к лечению и, возможно, даже вылечить ВИЧ-инфекцию.
Искренняя благодарность всем добровольцам, которые не пожалели своего времени на этот проект. И в то время как начальная фаза проекта FightAIDS@Home пришла к концу, убедитесь, что вкладываете во вторую фазу проекта.
Оригинал статьи